ou
Y a-t-il un atome à Bohr?
![]() LES
QUATRE ELEMENTS D'EMPEDOCLE D'AGRIGENTE
LES
QUATRE ELEMENTS D'EMPEDOCLE D'AGRIGENTE
De sa belle ville sicilienne d'Agrigente, le Grec Empédocle
(vers 492-432 av. J.-C.) divisa la matière en quatre éléments,
qu'il appela aussi "racines":
|
|
|
l'air |
|
Ces éléments sont mus par les forces de
l'amour et de la haine.
Dans l'amour absolu, ils forment une unité homogène,
alors que la haine les sépare. Lorsque ces deux forces entrent en
conflit, le mélange des éléments fait surgir les choses
matérielles.
Cette vision de la matière préfigure déjà
un peu la nôtre par la notion d'éléments liés
par des forces attractives et répulsives.
![]()
![]() LES
GRECS ATOMISTES
LES
GRECS ATOMISTES

Le mot "atome" vient du grec "a-tomos" et signifie "insécable".
Cette notion fut inventée par Leucippe de Milet en 420 avant
J.C.
![]() Son
disciple,
Démocrite d'Abdère (vers 460-370 av. J.-C.),
expliquait que la matière était constituée de corpuscules
en perpétuel mouvement et dotés de qualités idéales;
Ces corpuscules étaient:
Son
disciple,
Démocrite d'Abdère (vers 460-370 av. J.-C.),
expliquait que la matière était constituée de corpuscules
en perpétuel mouvement et dotés de qualités idéales;
Ces corpuscules étaient:
invisibles à cause de leur extrême petitesse insécables ou indivisibles comme leur nom l'indique pleins (pas de vide à l'intérieur) éternels car parfaits entourés d'un espace vide (pour expliquer le mouvement et les changements de densité) ayant une infinité de formes (pour expliquer la diversité observée dans la nature)
| L'atome est-il d'origine
grecque?
|
La doctrine atomiste greque sombra dans l'oubli pendant
de longs siècles et laissa place au triomphe durable de la théorie
des quatre éléments d'Empédocle.
![]()
![]() L'ALCHIMIE
DU MOYEN-AGE
L'ALCHIMIE
DU MOYEN-AGE
Née au Moyen-Age, l'alchimie est née
des progrès de la métallurgie et de l'insuffisance de la
théorie des 4 éléments à représenter
la diversité de la matière.
 Le
grand dessein de l'alchimie était d'obtenir la transmutation
des métaux "vils" (tels que le cuivre) en métaux "nobles"
tels que l'or. Sans doute parce que le succès du "Grand Oeuvre"
(la transmutation) ouvrait des perspectives de richesse et de pouvoir,
l'activité des alchimistes s'entourait de secret et s'inscrivait
dans une démarche très ancienne d'ésotérisme
et d'occultisme.
Le
grand dessein de l'alchimie était d'obtenir la transmutation
des métaux "vils" (tels que le cuivre) en métaux "nobles"
tels que l'or. Sans doute parce que le succès du "Grand Oeuvre"
(la transmutation) ouvrait des perspectives de richesse et de pouvoir,
l'activité des alchimistes s'entourait de secret et s'inscrivait
dans une démarche très ancienne d'ésotérisme
et d'occultisme.
La démarche de l'alchimie (comme celle de l'astrologie
d'ailleurs) établissait des liens symboliques qui unissaient le
microcosme au macrocosme (monde des planètes). Par exemple, l'élément
Plomb était associé à la planète Saturne car
celle-ci nous apparaît d'une couleur jaune "plombée".
Malgré leur croyance ésotérique,
les alchimistes développèrent l'observation, l'expérimentation,
la mesure et la classification des éléments: l'alchimie est
donc un précurseur respectable de la chimie. D'ailleurs n'oublions
pas que Newton en fut adepte et que la physique actuelle a réalisé
le vieux rêve de la transmutation en transformant certains atomes
en d'autres.
![]()
 En
1869, le chimiste russe Dimitri Mendeleïev construit un tableau
qui classe tous les éléments chimiques alors connus d'après
leurs propriétés chimiques. Ce tableau servira plus tard
à classer méthodiquement tous les atomes naturels et artificiels
d'après leur numéro atomique
(c'est-à-dire le nombre de leurs protons).
En
1869, le chimiste russe Dimitri Mendeleïev construit un tableau
qui classe tous les éléments chimiques alors connus d'après
leurs propriétés chimiques. Ce tableau servira plus tard
à classer méthodiquement tous les atomes naturels et artificiels
d'après leur numéro atomique
(c'est-à-dire le nombre de leurs protons).
![]()
![]() DECOUVERTE
DE L'ELECTRON
DECOUVERTE
DE L'ELECTRON
Et,
en 1897, Thompson découvre le premier composant de l'atome:
l'électron, particule de charge électrique négative.
En 1904, il propose un premier modèle d'atome,
surnommé depuis "le pudding de Thompson".
Il imagine l'atome comme une sphère remplie d'une
substance électriquement positive et fourrée d'électrons
négatifs "comme des raisins dans un cake".
![]()
![]() DECOUVERTE
DU NOYAU
DECOUVERTE
DU NOYAU
En
1912, Rutherford (physicien néo-zélandais) découvre
le noyau atomique.
Son nouveau modèle d'atome montre que sa charge
électrique positive, ainsi que l'essentiel de sa masse, est concentrée
en un noyau quasi-ponctuel.
Les électrons de l'atome se déplacent autour
de ce noyau tels des planètes autour du Soleil, et la force électrique
attractive (la charge - de l'électron attirant la charge
+ du noyau) joue le rôle de la force de gravitation pour les planètes;
d'où le nom de modèle d'atome planétaire.
A noter que contrairement à l'atome des Grecs,
celui de Rutherford n'est ni indivisible (puisque composite), ni plein
puisqu'il contient essentiellement du vide: La distance noyau-électrons
est 100.000 fois plus grande que le diamètre du noyau lui même
(diamètre du noyau = 10-15
mètre = 1 Fermi).
![]()
![]() DECOUVERTE
DES NUCLEONS
DECOUVERTE
DES NUCLEONS
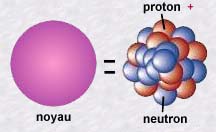
Rutherford comprend que le noyau est lui-même composé de nucléons. Ces nucléons sont de deux sortes:
Le modèle planétaire de l'atome présente
un gros défaut. Les électrons peuvent émettre de la
lumière sous certaines conditions (dans un ampoule électrique
par exemple); ce faisant, ils perdent de l'énergie et devraient
donc se rapprocher dangereusement du noyau jusqu'à s'y écraser!
Un tel atome ne serait donc pas stable.
![]()
![]() L'ATOME
DE BOHR
L'ATOME
DE BOHR
Afin
de rendre compte de cette stabilité atomique, Niels Bohr
crée en 1913 un nouveau modèle d'atome:
Les orbites des électrons ne sont pas quelconques
mais "quantifiées"; seules certaines orbites particulières
sont permises pour l'électron. Ce n'est que lorsque celui-ci saute
d'une orbite à l'autre qu'il peut émettre (ou absorber) de
la lumière.

![]()
![]() VERS
LA PHYSIQUE QUANTIQUE
VERS
LA PHYSIQUE QUANTIQUE
Le modèle de Bohr est le dernier modèle obéissant à la physique classique, c'est-à-dire la physique qui explique les mouvements et les phénomènes existant à notre échelle humaine. Ces modèles d'atomes sont donc faciles à comprendre et à se représenter.
 Quel
plaisir intellectuel (et quelle paresse!) que de se représenter
les atomes sous forme de petites boules tournant les unes autour des autres...
Quel
plaisir intellectuel (et quelle paresse!) que de se représenter
les atomes sous forme de petites boules tournant les unes autour des autres...
Ce modèle est d'ailleurs toujours celui que le
grand public affectionne!
Eh bien ce modèle est faux car, à l'échelle
atomique, de nouvelles lois s'appliquent! Ces lois appartiennent à
une étrange physique très éloignée de nos concepts
habituels: la
physique quantique.
![]()
![]() Avant de
continuer notre descente vers les constituants du noyau en découvrant
ce qu'est la physique quantique et ses conséquences sur la représentation
atomique, faisons le point sur ce que les physiciens savaient de l'atome
dans les années 1930:
Avant de
continuer notre descente vers les constituants du noyau en découvrant
ce qu'est la physique quantique et ses conséquences sur la représentation
atomique, faisons le point sur ce que les physiciens savaient de l'atome
dans les années 1930:
Pour les paresseux et en exclusivité mondiale: le crazyflash, un résumé déjanté de la page web:
Il est recommandé de lire
(avec un verre d'aspirine) le chapitre correspondant au crazyflash, afin
de saisir la substantifique moelle des jeux de mots et d'éviter
les jeux de maux de tête...
|
|
|